

























此前,“袁来如此”专栏就抗體(tǐ)药物(wù)和靶标生物(wù)分(fēn)析数据的具體(tǐ)应用(yòng)以及mAb和L的结合可(kě)能(néng)产生的问题展开了详细介绍(袁来如此|大分(fēn)子生物(wù)分(fēn)析概论(七_)上:LBA测定抗體(tǐ)药物(wù)与其靶标的总/游离浓度),本期将延续上期内容,重点关注抗體(tǐ)药物(wù)的定量和靶配體(tǐ)的生物(wù)分(fēn)析方法。
“袁来如此”专栏系广州博济医药微信公众号打造的科(kē)普學(xué)术专栏,内容均為(wèi)博济医药子公司深圳博瑞副总经理(lǐ)袁智博士原创。
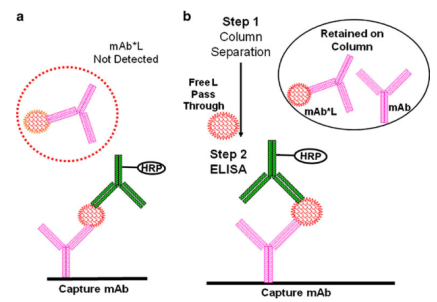
虽然可(kě)以设计LBA用(yòng)来测量mAbfree或mAbtotal,但受试剂限制、样本稀释等影响,并不能(néng)确定该方法是否仅仅测定mAbfree。因此,可(kě)以采取测定mAbtotal的策略。mAbtotal和mAbfree的分(fēn)析方法见表6,典型的ELISA检测格式见图2。
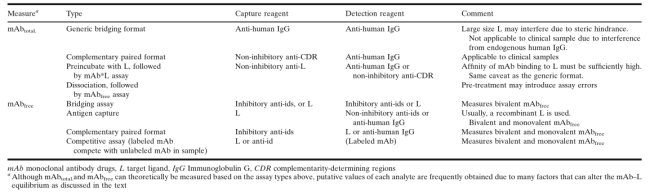
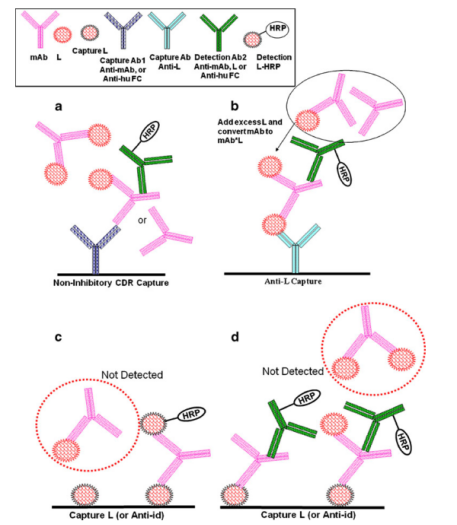
由于特异性试剂通常是不可(kě)及的,所以在临床前阶段通常采用(yòng)测定mAbtotal的“通用(yòng)”分(fēn)析方法。為(wèi)了与试验物(wù)种IgGs的交叉反应最小(xiǎo)化,可(kě)以使用(yòng)抗轻链(anti-light-chain)和/或亚型特异性(subclass-specific)试剂(例如图2的a、b使用(yòng)抗Fc试剂)。同样的方法可(kě)以用(yòng)于多(duō)种动物(wù)和不同的候选药物(wù),但是对于每个物(wù)种,仍然需要验证每个mAb方法。
“通用(yòng)”分(fēn)析方法可(kě)以作為(wèi)一种“现成的(off-the-shelf)”方法使用(yòng),在早期开发中,仅需要很(hěn)少的优化(在确定特定的测试试剂之前)。然而,这种格式的分(fēn)析方法不适用(yòng)于临床样本的检测,因為(wèi)其中含有(yǒu)mg/mL级别的人體(tǐ)内源性IgG的干扰,需要外加待测物(wù),回收实验评价来确认无内源性组分(fēn)的干扰。此外,该方法对活性(active)mAb药物(wù)没有(yǒu)特异性,但可(kě)能(néng)会与变性了的(denatured)、化學(xué)或蛋白酶降解后的mAb发生反应。
互补配对的格式使用(yòng)的非抑制性抗CDR抗體(tǐ)试剂(抗體(tǐ)试剂识别mAb超可(kě)变區(qū)域上不参与L结合位点的抗原表位)和通用(yòng)试剂方法是一种可(kě)以用(yòng)于临床样本的检测方法(例如,图2a使用(yòng)anti-mAb试剂)。在临床样本中,这种互补决定區(qū)域(complementarity-determining regions,CDR)的抗原表位不会出现在内源性人类IgG上。但是却很(hěn)难获得这样的non-inhibitory anti-CDR mAb试剂。另外,如果使用(yòng)多(duō)克隆抗體(tǐ)试剂,在药物(wù)开发项目的生命周期中,维护试剂批次间的一致性也是一个挑战。
对特异于mAbfree的测试格式,一对试剂中至少有(yǒu)一个试剂必须与待测物(wù)的同一位点结合。这些试剂可(kě)能(néng)是与L竞争结合的anti-idiotypic抗體(tǐ)(即inhibitory anti-ids)或者是L本身(图2c, d)。这种分(fēn)析方式的一个变种源自试剂的组合应用(yòng)(例如,“桥接bridging”格式中,使用(yòng)相同的试剂捕获和检测mAb,L作為(wèi)捕获试剂,与anti-idiotypic抗體(tǐ)进行结合检测,反之亦然)。桥接格式的一个优点是為(wèi)了能(néng)够被检测到,mAb必须要有(yǒu)两个functionally free结合位点。使用(yòng)L的捕获方式要求mAb只有(yǒu)一个供检测的游离结合位点,并且对游离和部分(fēn)游离的药物(wù)都有(yǒu)特异性。但分(fēn)析结果并没有(yǒu)揭示这两种形式的相对比例。

在mAbfree的竞争式分(fēn)析格式中,标记的mAb(例如biotin或horseradish peroxidase标记的)允许与样本中未标记的mAb竞争,以结合特定的捕获试剂。标记的mAb的数量将与样本中mAb的数量成反比。但是竞争式方法可(kě)能(néng)不如非竞争式方法的稳健性好。
虽然mAbfree代表拥有(yǒu)物(wù)活性的形式,是药代动力學(xué)家们的首选,但实际上,即使是设计良好的分(fēn)析方法,对體(tǐ)内mAbfree浓度的定量也存在着挑战性。正如《结合平衡和对mAbtotal/mAbfree分(fēn)析方法的挑战》中所讨论的,样品采集条件、处理(lǐ)过程或分(fēn)析方法都可(kě)以对平衡做出干扰影响,改变mAbfree的比例。
作為(wèi)替代方法,样品中mAbfree、Lfree和mAb-L的浓度可(kě)由mAbtotal和Ltotal来计算。但是计算是以平衡方程為(wèi)基础的,这需要对體(tǐ)内平衡解离常数(Kd)有(yǒu)很(hěn)好的估算。因為(wèi)动态平衡将随着不同的mAb和相应的L浓度而发生变化,所以需要在存在过量L的情况下检测mAb,然后根据经验判定它确实是mAbtotal或mAbfree的测试方法。
图3展示了测试L对mAb干扰的示例。以不同的摩尔比预孵育L和mAb,达到平衡后,用(yòng)特定ELISA来测定mAb的浓度。以L/mAb的摩尔比為(wèi)X轴,抑制率為(wèi)Y轴绘图。对于mAbfree的测定,IC50将接近1。但需要注意的是,用(yòng)于测试的重组L可(kě)能(néng)不能(néng)完全与其内源性形式一样地结合mAbfree,而导致IC50偏离真实值。
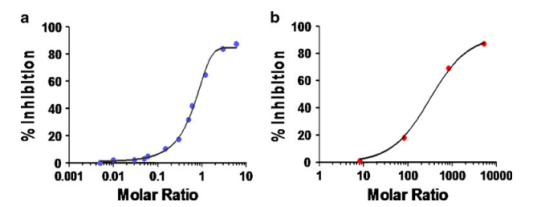
此外,选择一致和稳健的分(fēn)析方法来支持mAb产品的临床开发也很(hěn)重要。如果需要改变方法,应同时使用(yòng)外加药物(wù)的样本和真实的研究样本进行方法比较,以确定改变分(fēn)析方法对PK数据的影响。
Ltotal展示了有(yǒu)关mAb对L累积的影响的信息。由于mAb的半衰期通常比循环系统中L的半衰期長(cháng),给药后形成的mAb-L可(kě)能(néng)不会像Lfree那样快速清除。此外,在某些情况下,作為(wèi)给药后的响应,膜受體(tǐ)形式中L表达的上调或可(kě)溶性L的合成可(kě)能(néng)增加血液循环中L的浓度。
用(yòng)于Ltotal的分(fēn)析方法有(yǒu)多(duō)种。表7列举了相关方法并总结了这些方法的应用(yòng)和局限性。
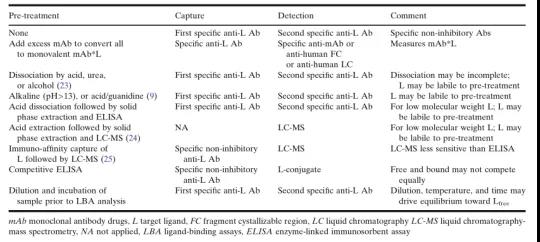
在给药过程中,监测Lfree对确定有(yǒu)效剂量具有(yǒu)重要意义。试剂的选择对Lfree分(fēn)析的影响与对mAbfree相似,但更加复杂。在许多(duō)情况下,与膜结合的L相比,组织中的可(kě)溶性L含量较低,可(kě)能(néng)需要高灵敏度的分(fēn)析方法来测定Lfree的正常水平。在大多(duō)数情况下,mAb/L的高摩尔比对给药后Lfree定量分(fēn)析的准确度造成了一定的阻碍。但即便如此,仍可(kě)获得Lfree的相对趋势,以提供有(yǒu)关mAb的影响和维持所需的Lfree水平等有(yǒu)价值的信息。
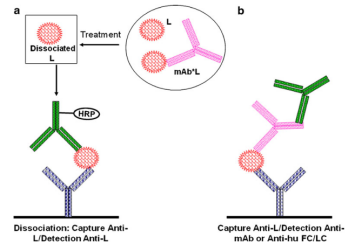
表8总结了临床前和临床阶段用(yòng)于测定Lfree的方法,图5展示了典型的测定Lfree的分(fēn)析方法。特异性的抑制性抗L抗體(tǐ)或mAb(或mAb模拟物(wù))可(kě)作為(wèi)捕获试剂,而特异性的非抑制性抗L抗體(tǐ)可(kě)作為(wèi)检测试剂(图5a)。但是解离结合形式的L(bound form of L)的样本处理(lǐ)步骤和分(fēn)析条件可(kě)能(néng)会导致检测值偏高(见《结合平衡和总/游离型分(fēn)析的挑战》)。

另一种方法是通过分(fēn)子筛、固相萃取或亲和分(fēn)离法,在LBA分(fēn)析之前,去除结合形式的L(图5b,如使用(yòng)G蛋白、A蛋白或抗人FC柱)。然而,由于柱子或过滤器表面的吸附作用(yòng),这些额外的步骤可(kě)能(néng)会带来误差,而且在这些分(fēn)离过程中也可(kě)能(néng)会发生解离。因此,Lfree的数据只能(néng)显示出相对的趋势,而不能(néng)作為(wèi)绝对的定量结果。
在使用(yòng)样本制备方法开发Ltotal和Lfree测定方法的时候,需要重点评估在预期浓度范围内的Lrecovery(L的回收率)以及在预期有(yǒu)或没有(yǒu)mAb的基质中,评估来自样本基质和其它相关结合蛋白的干扰。重要的是要确认在使用(yòng)最终方法时测定的值是Ltotal还是Lfree。可(kě)以采用(yòng)不同mAb/L摩尔比进行干扰测试,类似于图3所示的实验。

测定靶标配體(tǐ) (Ltotal或者Lfree)可(kě)以提供一些重要的信息,包括证明mAb与L的體(tǐ)内结合、靶点占用(yòng)率、有(yǒu)效的mAb浓度以及PK/PD关系。
测定L的准确度取决于标准参照(比)物(wù)和试剂的质量。当不能(néng)获得内源性L的标准参照(比)物(wù)时,可(kě)以使用(yòng)重组或合成的L标准参照(比)物(wù)。定量的准确度取决于标准参照(比)物(wù)与内源性待测物(wù)这二者与测试试剂结合的相对活性(relative binding activity)。
在分(fēn)析方法验证的过程中,应评估Ltotal的平行性,以确定该方法是否能(néng)像标准参照(比)物(wù)一样识别内源性的L。如果缺乏平行性数据,该分(fēn)析方法只能(néng)是半定量的,所产生的数据必须在此背景下进行解释。当没有(yǒu)足够高浓度的内源性L样本来评估平行性时,解释数据时应该谨慎使用(yòng)绝对浓度这样的术语。在这种情况下,L的相对变化趋势将更加可(kě)靠。
為(wèi)了适当地使用(yòng)和解释生物(wù)分(fēn)析数据,了解数据的可(kě)靠性和局限性是至关重要的。在LBA方法中,捕获和检测试剂是决定该方法的特异性(针对游离的、结合的或总浓度的特异性)的关键组成成分(fēn)。理(lǐ)解mAb/L的比值和动态平衡对于选择最合适的格式进行方法开发是至关重要的。
此外,在疾病模型或特定患者群體(tǐ)中,靶标配體(tǐ)的状况可(kě)能(néng)与健康对照群體(tǐ)有(yǒu)着非常不同的情况,所以了解在不同物(wù)种和疾病状态中出现的mAb/L比值的可(kě)变性也很(hěn)重要。即使拥有(yǒu)高度表征的试剂,也应该理(lǐ)解mAb-L在體(tǐ)内是以动态平衡的方式存在的,因此體(tǐ)外(ex vivo)的测试条件(例如样本稀释和孵育时间)会影响mAb和L的定量以及它们两者之间的平衡,可(kě)以通过研究mAb-L平衡,分(fēn)析操作步骤,评估实验结果,来判断它们是否真实反映了研究样本中的结合关系(binding relationships)。本文(wén)的表格中所列出的样品处理(lǐ)策略和定量方法,经常适用(yòng)于方法开发,其目的是定量分(fēn)析游离(free)的、总體(tǐ)(total)的和结合了(bound)的mAb和L的各种形式。
mAb和L的浓度数据一般用(yòng)来在药物(wù)开发的不同阶段帮助做出具體(tǐ)的决策。在临床前研究中,可(kě)能(néng)没有(yǒu)相关试剂用(yòng)于开发定量mAbfree的方法。mAbfree和mAbtotal(当没有(yǒu)检测mAbfree的方法时)的定量数据将用(yòng)于评估系统暴露量-时间过程与毒性研究结果的关系,并预测人體(tǐ)起始剂量的安全余量。通常情况下,mAb给药的剂量会使得血液中mAb的浓度遠(yuǎn)超L,因而mAbtotal与mAbfree相近并可(kě)以作為(wèi)mAb活性的指标,进而基于PK-PD模型计算来决定采用(yòng)多(duō)大剂量。
在临床评估中,会使用(yòng)特定试剂测定mAbfree或mAbtotal以描述mAb药物(wù)在人體(tǐ)中的分(fēn)布情况,并将mAb的暴露量与其安全性和有(yǒu)效性联系起来。同时,也有(yǒu)助于更好地理(lǐ)解mAb-L的动力學(xué),為(wèi)后期临床研究时选择给药方案提供相关信息。
在药物(wù)开发中,越来越多(duō)的研究人员选择使用(yòng)靶标配體(tǐ)(L)的浓度数据来指导决策。例如,Lfree的数据可(kě)用(yòng)于指导给药剂量和频率的选择。对L动力學(xué)的理(lǐ)解有(yǒu)助于确定维持受體(tǐ)占用(yòng)率所需的mAbfree的有(yǒu)效浓度。在许多(duō)情况下,由于Lfree的浓度很(hěn)低,并且可(kě)能(néng)随分(fēn)析条件的变化而变化,定量数据可(kě)能(néng)是不可(kě)靠的。
另一种方法是考查给药后Lfree的变化趋势,而不是依赖其绝对值。Ltotal提供了mAb活性的证据,此外,如果mAb–L的结合改变了靶点表达量(例如L的高度积累),可(kě)能(néng)需要提醒研究人员注意安全性的问题。可(kě)以在PK/PD模型中,使用(yòng)Ltotal来推断Lfree的浓度。根据Ltotal、Lfree以及mAbfree或者mAbtotal的适当信息,通过PK/PD建模来估计Lfree的體(tǐ)内结合亲和力和抑制作用(yòng),这可(kě)能(néng)有(yǒu)助于给药剂量和频率的选择。
由于待测物(wù)的形态(游离/总/复合,free/total/complex)和用(yòng)于定量这些形态的生物(wù)分(fēn)析方法会影响药物(wù)暴露量-时间过程的确定,因此在整个药物(wù)开发计划的背景下,对生物(wù)分(fēn)析数据的解释保持一致是至关重要的。
此外,设计能(néng)够解决相关科(kē)學(xué)问题的生物(wù)分(fēn)析方法也很(hěn)重要。由于每个靶标及其相关疾病生物(wù)學(xué)的复杂性和独特性,应与数据的最终用(yòng)户协商(shāng),為(wèi)每个药物(wù)开发项目精心制定定量相关形式的生物(wù)分(fēn)析策略,并考虑药物(wù)靶标生物(wù)學(xué)、药物(wù)开发阶段和包括试剂可(kě)及性在内的实际挑战。当前满足所有(yǒu)要求且令人满意的生物(wù)分(fēn)析方法少之又(yòu)少,还需要更多(duō)的努力来开发相关方法,所以目前大多(duō)数情况下只能(néng)使用(yòng)不太理(lǐ)想的分(fēn)析方法来支持药物(wù)开发的某个阶段。在这种情况下,应该清楚地向所有(yǒu)利益攸关方传达使用(yòng)不太理(lǐ)想的分(fēn)析方法时的注意事项、对数据的影响和项目的相关风险,以确保做出恰当的决策。
在一些文(wén)献中,有(yǒu)些學(xué)者使用(yòng)串联高效色谱-质谱(LC-MS/MS)方法来定量mAb。此种方法涉及酶消化,将mAb转化成小(xiǎo)的肽段(以保持在一定的质荷比范围内)。需要注意的是,mAb必须在酶消化前变性,确保mAb与L的分(fēn)离。因此,LC-MS/MS方法可(kě)用(yòng)于定量mAbtotal。用(yòng)于蛋白质定量的LC-MS/MS方法将在后续文(wén)章中探讨。
虽然本文(wén)所述的问题和例子可(kě)适用(yòng)于多(duō)种类型的生物(wù)药,但為(wèi)了明确起见,本文(wén)重点关注的是mAb及其相关的靶标配體(tǐ)L。对于其它生物(wù)药的复杂性,如蛋白质、肽和寡核苷酸及其相互作用(yòng),还需要进一步考虑扩展这里提出的概念,并在未来探讨。
就实际的分(fēn)析方法开发和结果数据的适当运用(yòng)而言,提出明确和果断的建议是一个巨大的挑战。本文(wén)试图确定在药物(wù)开发的每个阶段数据的合用(yòng)性,以便开发可(kě)以用(yòng)于特定目的的定量分(fēn)析方法。更重要的是强调了分(fēn)析方法的局限性(对于适当地解释和使用(yòng)数据而言)。后续有(yǒu)机会将继续探讨mAbs和非mAbs生物(wù)药的相关问题和挑战,如结合mAb的抗药物(wù)抗體(tǐ)(ADA),敬请关注。
本文(wén)如有(yǒu)疏漏和误读相关指南和数据的地方,请读者评论和指正。所有(yǒu)引用(yòng)的原始信息和资料均来自已经发表學(xué)术期刊、 官方网络报道等公开渠道, 不涉及任何保密信息。参考文(wén)献的选择考虑到多(duō)样化但也不可(kě)能(néng)完备。欢迎读者提供有(yǒu)价值的文(wén)献及其评估。

