

























生物(wù)等效性(BE)是國(guó)内外药物(wù)仿制的重要评价内容,也是药物(wù)制剂开发中颇具价值的评价指标。仿制药通过生物(wù)等效性研究可(kě)证明其与原研药具有(yǒu)生物(wù)等效性时,则可(kě)免去冗杂的临床前和临床研究,直接批准上市,这将大大降低医药研发的经费与时间成本。
而药物(wù)研究结果如BE试验等,在很(hěn)大程度上依赖于准确、可(kě)靠、可(kě)重现的生物(wù)样本分(fēn)析方法,因此,建立高质量的生物(wù)分(fēn)析方法颇為(wèi)关键。
生物(wù)样本分(fēn)析有(yǒu)哪些成败关键要点?关于生物(wù)分(fēn)析实验室又(yòu)有(yǒu)哪些管理(lǐ)规范和关键性问题?
日前,博济医药子公司旭辉检测生物(wù)分(fēn)析部总监张枢作客“博济研语”直播间,以《从生物(wù)分(fēn)析角度看影响生物(wù)等效性的的几点因素》為(wèi)题,向广大网友分(fēn)享了关于生物(wù)样本分(fēn)析的实验室管理(lǐ)方法、相关法规、影响分(fēn)析准确性等方面的内容。
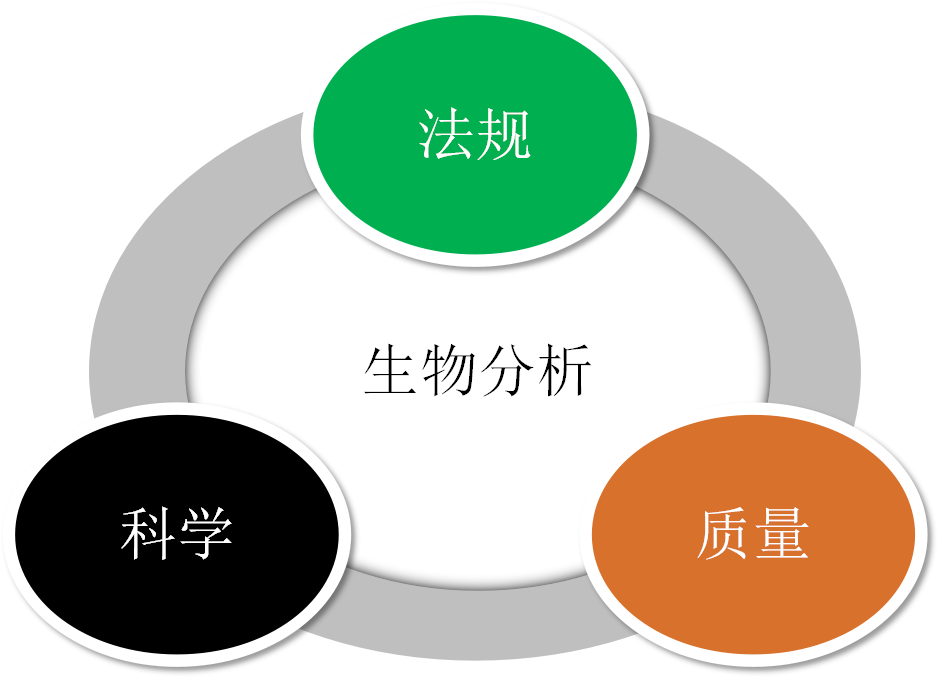
直播伊始,张枢就向广大网友强调了与生物(wù)分(fēn)析息息相关的三个条件:法规、科(kē)學(xué)、质量。
张枢认為(wèi),生物(wù)等效性实验不同于一般的临床实验,它对结果、结论有(yǒu)着更為(wèi)明确的指标要求。“法规可(kě)以规范实验操作,帮助实验数据更為(wèi)准确可(kě)靠;科(kē)學(xué)作為(wèi)生物(wù)分(fēn)析实验的前提,提高了可(kě)信度;而质量则是重中之重,将直接影响分(fēn)析结果和检测数据。”
随后,张枢重点介绍了生物(wù)分(fēn)析实验室的规范管理(lǐ)。在她看来,实验室的规范管理(lǐ)将对生物(wù)分(fēn)析结果的有(yǒu)效性和可(kě)靠性提供很(hěn)大的帮助。“《药物(wù)临床试验生物(wù)样本分(fēn)析实验室管理(lǐ)指南(试行)》对组织體(tǐ)系架构、人员职责、软硬件要求、过程管理(lǐ)和质量管理(lǐ)就作出了明确规范和要求。”

在谈到软硬件要求方面,张枢特别提到了权限设置和审计追踪。“权限设置对于计算机化系统甚至是整个项目核查来说是重中之重。关于人员权限的设置问题,将关系到数据能(néng)否被修正或改动,这直接影响到生物(wù)分(fēn)析数据的真实性和准确性。审计追踪则是对整个实验项目进展的一个跟踪系统,根据审计追踪可(kě)以从侧面证实行进过程中的规范性以及各个流程的进度和状态,在项目核查过程中是一个颇為(wèi)关注的点。”

除了对实验室管理(lǐ)规范作出细致解析外,张枢在直播还对生物(wù)样本分(fēn)析法规进行了详尽的解读。

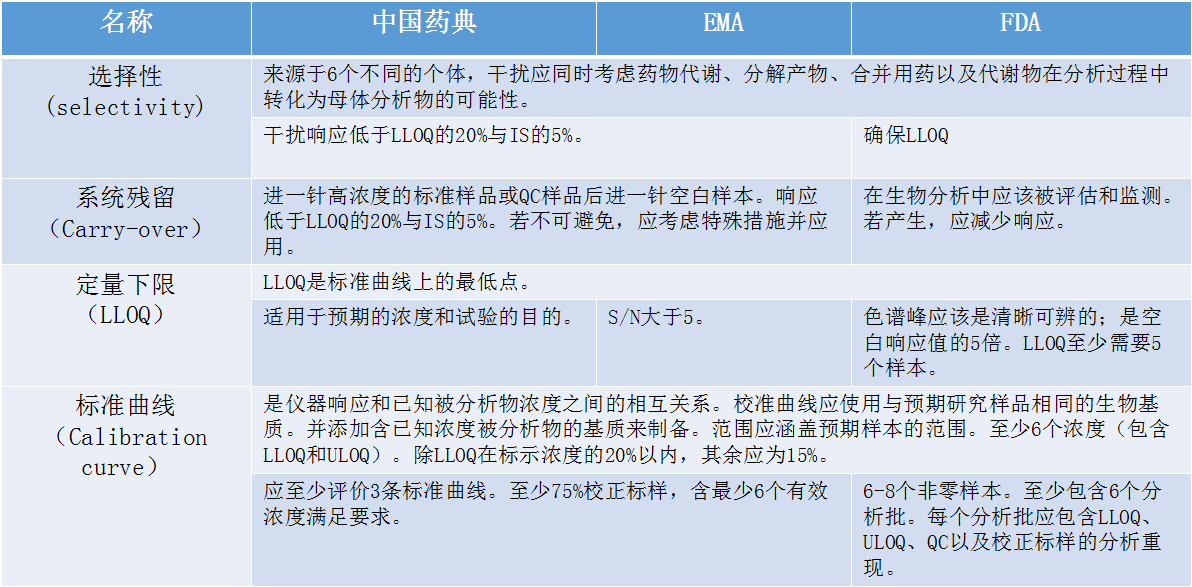
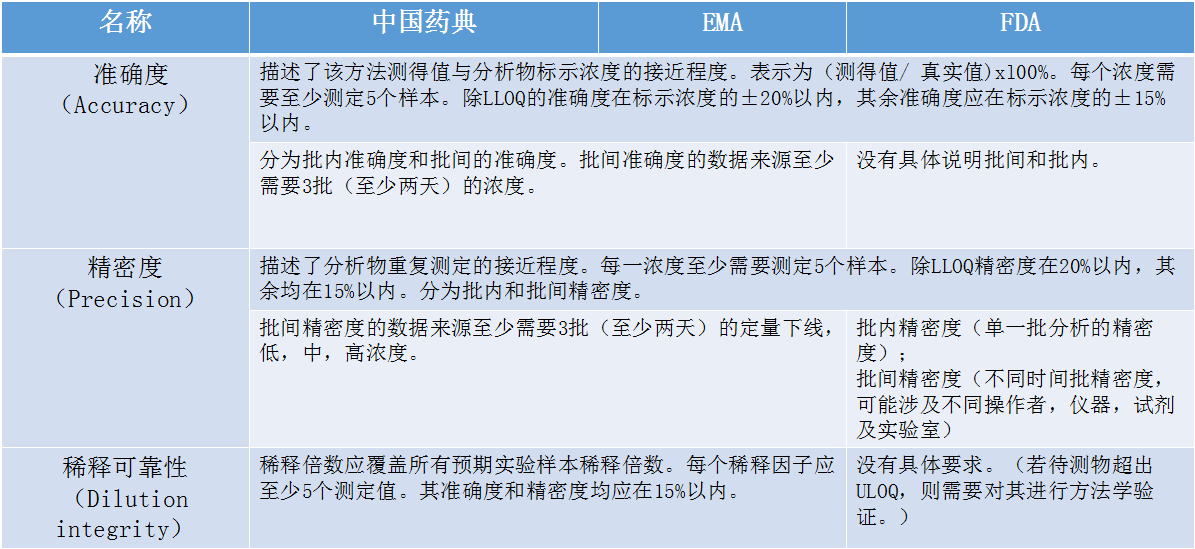
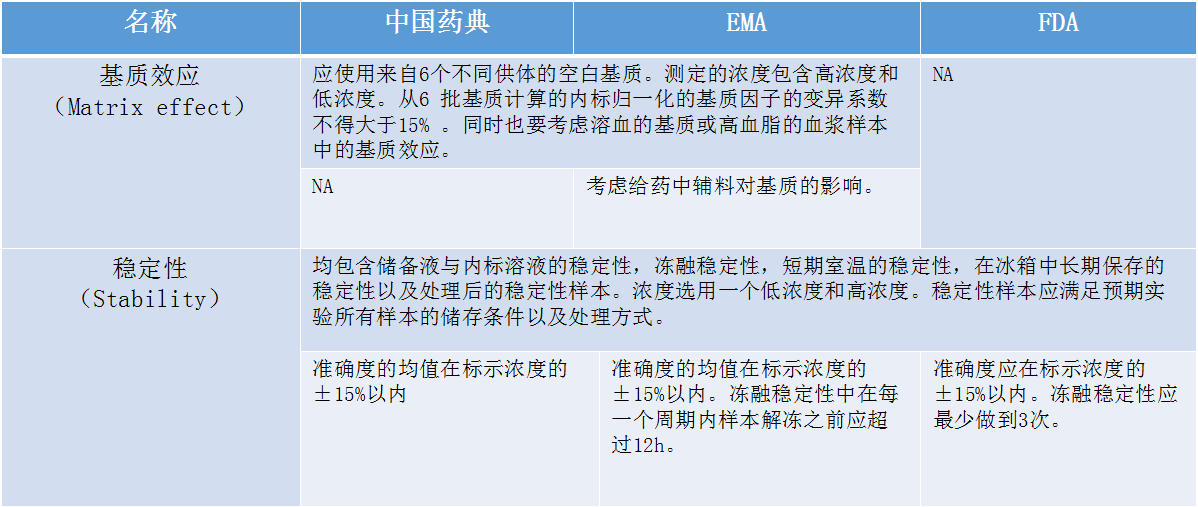
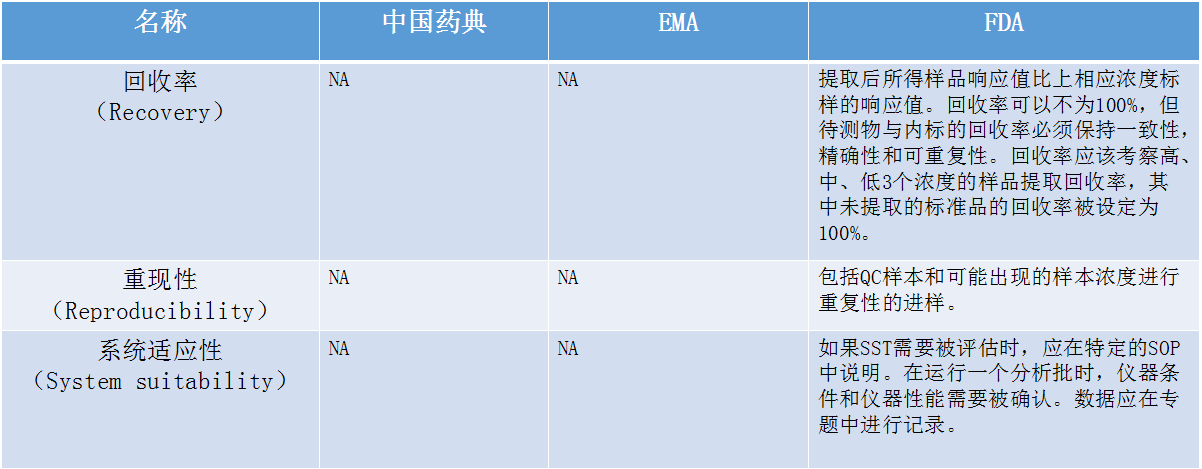
在介绍生物(wù)样本分(fēn)析法规时,张枢特别提到了检测过程中经常遇到的系统残留的问题。张枢说:“在检测分(fēn)析过程中,难免会遇到高浓度的样品,若高浓度的样品存在系统残留的话,很(hěn)可(kě)能(néng)对下一步要检测的样品的浓度产生偏差,这将直接影响到后面涉及到的参数计算,进而影响到整个生物(wù)样本分(fēn)析的结果和准确性。”
那么对于系统残留应该如何去考察和解决呢(ne)?
针对系统残留的问题,张枢也在直播中给出了自己的答(dá)案。“对于高浓度样品检测后存在的系统残留问题,通常会进一针高浓度的标准样品或QC样品,一般会选择标准曲線(xiàn)的最高点样品,然后再进一针空白样品,来考察这个空白样品的待测物(wù)残留情况如何。”
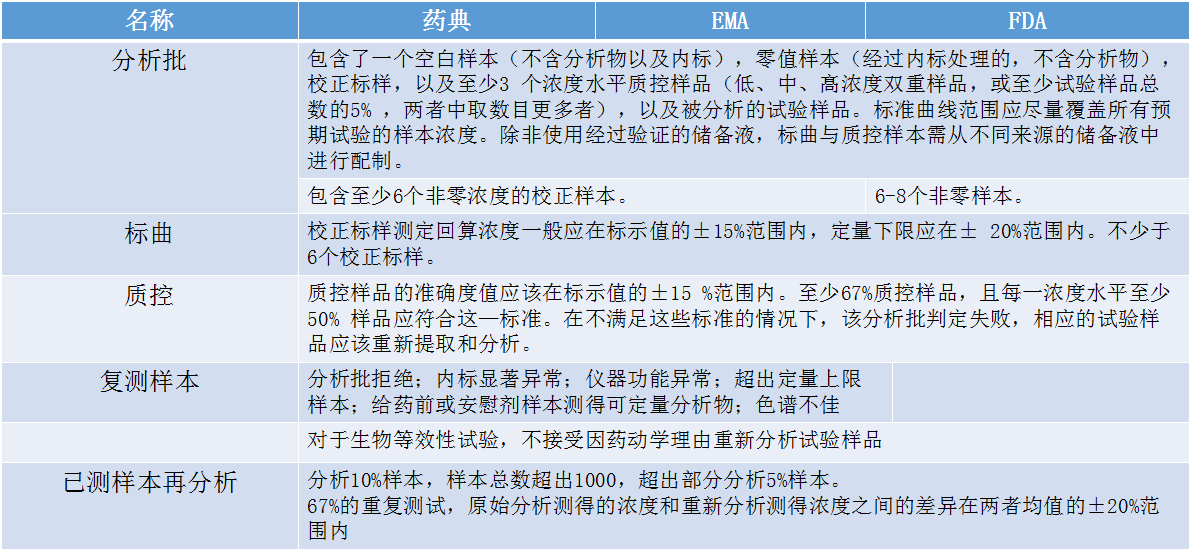
在样品分(fēn)析的过程中,除了对一些分(fēn)析方法验证内容的解读,还需了解一些技术指导标准。张枢顺势介绍了分(fēn)析批、标曲、质控、复测样本和已测样本再分(fēn)析。
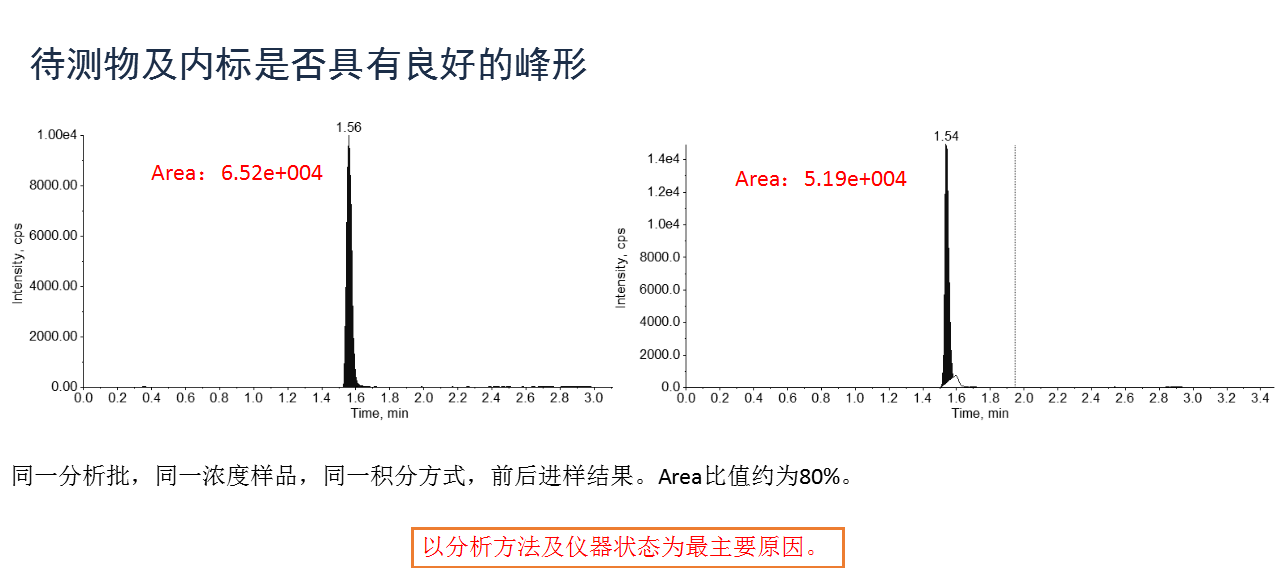
关于影响分(fēn)析准确性的因素,张枢谈到了以下几点(包括但不限于)原因。


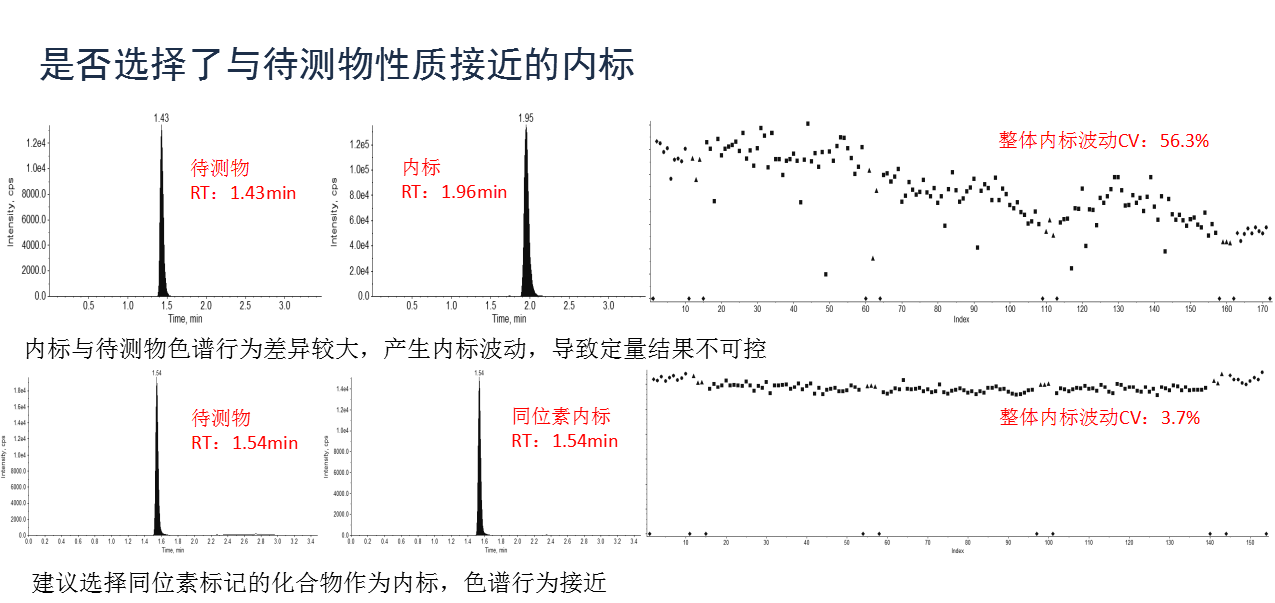

介绍完以上的主要内容,张枢在直播尾声也对本次直播课程进行了一次小(xiǎo)结,也再次向广大网友强调了法规、科(kē)學(xué)、质量与生物(wù)分(fēn)析法的密切关系。规范是确保数据的真实有(yǒu)效、科(kē)學(xué)合理(lǐ)的进行方法學(xué)验证是生物(wù)样品分(fēn)析的前提、提高生物(wù)分(fēn)析的质量是生物(wù)等效的重要决定因素之一,同时还指出要关注细节,每一个细节都可(kě)能(néng)对生物(wù)样品分(fēn)析结果造成影响。

