新(xīn)药研发是一个经历播种、开花(huā)、“梦想”结果的系统工程。随着中國(guó)加入ICH,中國(guó)医药工业跃入了世界的竞争舞台中,创新(xīn)药实现“全球新(xīn)”是必然趋势。实现新(xīn)药研发的國(guó)际化,首先离不开源头的水即企业内部的技术开发能(néng)力,其次离不开外部团队的专业协助。多(duō)方位的准确、及时和可(kě)靠的专业技术咨询,以达到國(guó)外的法规要求,才能(néng)实现开花(huā)(即IND),直至收获最后的结果(即NDA)。而这中间需要搭桥者,需要引路人!这正是美國(guó)汉佛莱医药顾问有(yǒu)限公司首席顾问杜涛博士一直在做且愿意花(huā)一辈子去做的一件事:帮助中國(guó)医药企业走向國(guó)际化,做实现“全球新(xīn)”的引路人。

杜涛博士
现任美國(guó)汉佛莱医药顾问有(yǒu)限公司首席顾问和中國(guó)區(qū)总经理(lǐ) 。國(guó)家级高级人才,美國(guó)医药工业的知名顾问。曾带领来自不同國(guó)家、有(yǒu)着不同文(wén)化背景和不同专业特長(cháng)的新(xīn)药开发团队成功地完成了60多(duō)项新(xīn)药开发和申报工作。其中包括多(duō)家中國(guó)制药企业在美國(guó)开发的植物(wù)药,生物(wù)药,化學(xué)新(xīn)药和化學(xué)仿制药。他(tā)所形成的一些药品开发和注册策略/技术方案在北美制药行业中有(yǒu)着相当大的影响。
一
追求“一流水平”的心态
“在一个状态下,你追求的是二流水平,结果你达到的一般是三流水平;你追求的是一流水平,结果达到可(kě)能(néng)是二流水平也有(yǒu)可(kě)能(néng)是一流水平。所以,尽可(kě)能(néng)追求卓越”,在學(xué)术科(kē)研道路上,杜博士一直在挑战自我和不断探索。
从天津医科(kē)大學(xué)毕业后留學(xué)美國(guó),杜博士凭借不懈的努力,成功进入了被称為(wèi)“加拿(ná)大哈佛”的世界名校——麦吉尔大學(xué)(McGill University),攻读病理(lǐ)學(xué)博士。由于是McGill的毕业生和曾发表的高质量文(wén)章,他(tā)顺利申请到了哈佛大學(xué)病理(lǐ)系两年博士后训练的机会。
在哈佛医學(xué)院深造期间,他(tā)见证了一项候选药物(wù)从实验室走向一期临床开发全部过程,體(tǐ)会到药物(wù)开发是一个需要多(duō)學(xué)科(kē)参与的协作过程。这一切激发了他(tā)对医药开发的浓厚兴趣。
二
FDA的沉淀,知道了什么是监管科(kē)學(xué)
对杜博士来说,最大的动力就是不断有(yǒu)新(xīn)知识可(kě)以學(xué)习,尤其是医药工业开发相关的。
“作為(wèi)医生,他(tā)只是在使用(yòng)药,可(kě)能(néng)并不理(lǐ)解这个药是怎么开发研究出来的,FDA的申报作為(wèi)药物(wù)研发流程的最后一个阶段,是对整个药物(wù)研发流程的把控,乃至对这个领域的洞察监管,这当中涉及的知识是博大精深的,有(yǒu)很(hěn)多(duō)东西也是自己从不知道的,可(kě)以學(xué)到很(hěn)多(duō)东西,可(kě)以做很(hěn)多(duō)事情……”于是两年博士后训练之后,杜博士坚定的选择进入了FDA这个平台作為(wèi)起点。
“正是由于在FDA的工作经历,使我懂得了什么是监管科(kē)學(xué)” 杜博士在FDA的工作是一个快速成長(cháng)和收获的经历。在FDA工作的7年间,杜博士担任高级审评官员,审评过一百多(duō)个药品的IND和NDA。也多(duō)次获得美國(guó)政府颁发的奖励,包括对FDA植物(wù)药指南文(wén)件起草(cǎo)工作做出了很(hěn)大贡献,获得过FDA Commendable Service Award。
医药工业是一个具有(yǒu)进展性特点的行业。通俗讲来说,今天认為(wèi)一个正确的事,十年以后就不太正确了,二十年以后就认為(wèi)可(kě)以被淘汰了。比如“仿制药热潮”经历时代的变化,大浪淘沙,一致性评价成為(wèi)了关键。这也正是这个行业的魅力所在,需求在增加,科(kē)學(xué)在进步,就会逼着知识在增加,总有(yǒu)學(xué)不完的东西。“医药工业这个行业太有(yǒu)意思了,我愿意呆一辈子”不断接受新(xīn)知识的杜博士,已经对FDA的监管科(kē)學(xué)有(yǒu)了深刻的理(lǐ)解,对药品开发、注册相关的策略和技术方案有(yǒu)了一定的认知。
三
转入药企实践,精修内功
2000年,杜博士再一次挑战,离开了服務(wù)多(duō)年的FDA,“深入到企业实践去,医药研发还有(yǒu)很(hěn)多(duō)东西要學(xué),还有(yǒu)很(hěn)多(duō)事情要做。”,杜博士先后担任美國(guó)联合健保公司的中國(guó)區(qū)首席代表和全球注册部高级总监,以及香港和记黄埔医药的临床和注册部高级总监,接近五年的实战经验中,杜博士对医药研发有(yǒu)了更深入的理(lǐ)解,并进一步深化形成自己独特的药品开发、注册相关的策略和技术方案。
2005年,杜涛博士进一步挑战,凭借之前积累的投资人脉和对医药开发的独特见解,加入了美國(guó)汉佛莱顾问有(yǒu)限公司担任顾问,走进医药金融顾问行业,当时主要在华尔街(jiē)做顾问,实际上就是帮助医药企业去解释自己的技术,帮助投资机构去理(lǐ)解医药企业的产品和开发计划。这当中核心能(néng)力是对医药开发流程和技术的理(lǐ)解。“顾问”这个特殊角色的任務(wù)就是搭建了医药和资本之间的沟通桥梁,促使投资工业找到合适的医药项目,也帮助有(yǒu)价值的医药研发项目得到资本的支持。
在担任顾问期间,杜博士还担任过了三家在北美上市公司的独立董事和两家美國(guó)的专利事務(wù)所的医药技术顾问。 在这几年的实践过程中, 他(tā)深切的感受到, 无论是一个重要新(xīn)药的上市,还是一个伟大药企的成功都离不开幕后的重要推手——资本。融资和上市对于一家医药企业的作用(yòng)不亚于一项试验室内的新(xīn)药发明和一个成功的临床试验。这不禁让他(tā)感叹, 对人类生命如此重要的医药工业真是太博大精深了。
2008年美國(guó)次贷危机之后,杜博士正式回归医药工业担任顾问,也就是工作重心又(yòu)转换到专注于医药法规和医药开发的顾问角色上。他(tā)带领来自不同國(guó)家、有(yǒu)着不同文(wén)化背景和不同专业特長(cháng)的新(xīn)药开发团队成功地完成了一系列新(xīn)药开发和申报工作。至今,他(tā)所形成的一些药品开发、注册相关的策略及技术方案在北美制药行业中有(yǒu)着相当大的影响。
四
回國(guó),肩负起使命
“医药工业这个行业,我愿意呆一辈子”,着迷于医药工业的杜博士已经精修一身内功,并于2012年入选國(guó)家高层次人才,作為(wèi)海归人才,他(tā)深切意识到帮助中國(guó)医药工业走向國(guó)际化的使命感。
美國(guó)FDA的药审政策和标准一直被视為(wèi)國(guó)内外药政法规部门和药企的重要参考,能(néng)否通过FDA的审批也自然成為(wèi)衡量制药企业是否与國(guó)际接轨的重要标准之一。但是当时中國(guó)还没有(yǒu)能(néng)够提供FDA申报服務(wù)的企业。“中國(guó)医药工业走向國(guó)际化需要搭桥者和引路人”,作為(wèi)美國(guó)汉佛莱医药顾问有(yǒu)限公司合伙人,杜博士决定在中國(guó)设立全资子公司,并先后在北京设立办公室、南京成立南京禾沃医药有(yǒu)限公司。汉佛莱医药是首家拥有(yǒu)FDA電(diàn)子注册申报能(néng)力的中國(guó)公司,是注册CRO行业的探索者和先行者,专业為(wèi)医药工业提供高端技术服務(wù),包括FDA产品注册申报、临床试验监控、技术转让及项目评估咨询等多(duō)项服務(wù)。
在决心為(wèi)中國(guó)医药工业國(guó)际化的道路上,杜博士表示信心十足。海归人才是助力中國(guó)医药企业走向國(guó)际化的中坚力量,“近年来,有(yǒu)很(hěn)多(duō)FDA的华人前同事,也回到中國(guó),為(wèi)中國(guó)企业走向國(guó)际的提供各种申报咨询服務(wù),这给了我更大的信心。 有(yǒu)这些优秀的人才,中國(guó)产品进入世界主流医药市场将是一个毫无悬念的问题。”杜博士表示,汉佛莱医药拥有(yǒu)FDA前审评官员和行业专家组成的核心顾问团队。
2018 年 5 月,汉佛莱医药顾问团队和丽珠项目团队一起完成了一项重要的FDA的注册申报工作,共同推进了丽珠集团旗下的参芪扶正注射液成為(wèi)首个被FDA批准临床试验的中药复方注射剂。“项目成功获批临床主要得益于丽珠内部研发团队的贡献,也获得了外部专家的助力。医药工业走向國(guó)际化,离不开源头的水即企业内部的技术开发能(néng)力,其次离不开外部专家的协助,专家提供准确、全面可(kě)靠专业技术咨询,才能(néng)共同助力达到國(guó)外的法规要求,而我们就是企业可(kě)以寻求的外部助力中的一部分(fēn)。”杜博士对此解释到。
到今天為(wèi)止,作為(wèi)國(guó)内规模最大的, 专注于FDA申报咨询服務(wù)的团队,汉佛莱医药已经為(wèi)三十多(duō)家中國(guó)公司提供FDA申报服務(wù),项目成功率100%。成功的记录包括:第一个中國(guó)植物(wù)药的FDA临床申报;第一个植物(wù)复方注射剂的FDA临床申报;完成第一个活细菌的临床申报;第一个中國(guó)做双靶点抗體(tǐ)药物(wù)的FDA申报;第一个中國(guó)企业的CAR-T的FDA申报……
五
加盟博济,深入中國(guó)市场
2015年,國(guó)務(wù)院出台《关于改革药品医疗器械审评审批制度的意见》拉开了改革的序幕,随后在國(guó)家一系列改革政策的推动下,中國(guó)医药工业全球化速度进入了崭新(xīn)的时代。博济医药作為(wèi)深耕临床前与临床研究服務(wù)的本土CRO公司,需要增强國(guó)际注册能(néng)力,帮助更多(duō)國(guó)内企业融入世界医药浪潮。2017年,杜涛博士基于与博济医药董事長(cháng)王廷春博士拥有(yǒu)共同的理(lǐ)念与追求,汉佛莱医药加盟博济医药,成為(wèi)博济医药的控股子公司。
“首先,我们理(lǐ)念是一致的,助力中國(guó)医药工业的國(guó)际化;其次,博济医药是具有(yǒu)全方位的完善的服務(wù)體(tǐ)系,在技术实力、服務(wù)质量等各个方面处于國(guó)内CRO行业的领先位置, 双方携手并进,将进一步深入中國(guó)市场,健全一站式新(xīn)药研发全产业链条服務(wù),满足國(guó)内企业走向國(guó)际化的需求”杜博士说到。
随着药品审评审批制度改革的不断深化,國(guó)内医药创新(xīn)风起云涌。企业开展國(guó)际合作能(néng)力不断增强,数家优秀企业同步在海外开展临床试验。汉佛莱医药在博济医药的带领协同下,服務(wù)网络得到了进一步推进。
面对高速发展的中國(guó)医药工业,杜涛博士表示,汉佛莱医药的创建具有(yǒu)深遠(yuǎn)且重要的意义,汉佛莱医药要做的就是中國(guó)医药工业走向國(guó)际化的专业搭桥者,提供完整全面专业的國(guó)际医药注册咨询服務(wù)。
对杜博士来讲,不断學(xué)习,做实现医药“全球新(xīn)”的引路人,就是最重要的事。2017年—2019年参与策划同写意新(xīn)药中美双报系列论坛,為(wèi)中國(guó)新(xīn)药的FDA之路接力领航;加入清华大學(xué)药學(xué)院实战型导师团队,与國(guó)内外顶尖专家學(xué)者和企业家联袂打造清华大學(xué)药學(xué)院【创新(xīn)药物(wù)研发与产业化】课程,助力培养新(xīn)一代药學(xué)创新(xīn)人才;2011年起一直担任美國(guó)北卡罗来纳州立大學(xué)客座教授,向来自中國(guó)药监局,药典会和各省药检所的學(xué)员讲授FDA法规,以及新(xīn)药和仿制药在美國(guó)的开发策略……“既然决心在医药工业这个领域干一辈子,那就尽可(kě)能(néng)地去做更多(duō)的事”杜博士坚定的做了总结。

2017,2018和2019三年中美双报大会,杜涛博士均获 “最受欢迎的报告人”奖牌
相关链接
美國(guó)汉佛莱医药顾问有(yǒu)限公司
是一家专业為(wèi)医药工业提供高端技术服務(wù)的科(kē)技咨询公司。专业从事美國(guó)FDA注册、FDA申报、FDA咨询,以及其它國(guó)际医药注册等服務(wù)。目前是國(guó)内最大的FDA注册团队和商(shāng)业咨询团队,已完成100多(duō)项成功案例,是國(guó)内首家拥有(yǒu)FDA“電(diàn)子申报”能(néng)力的公司。
服務(wù)项目:
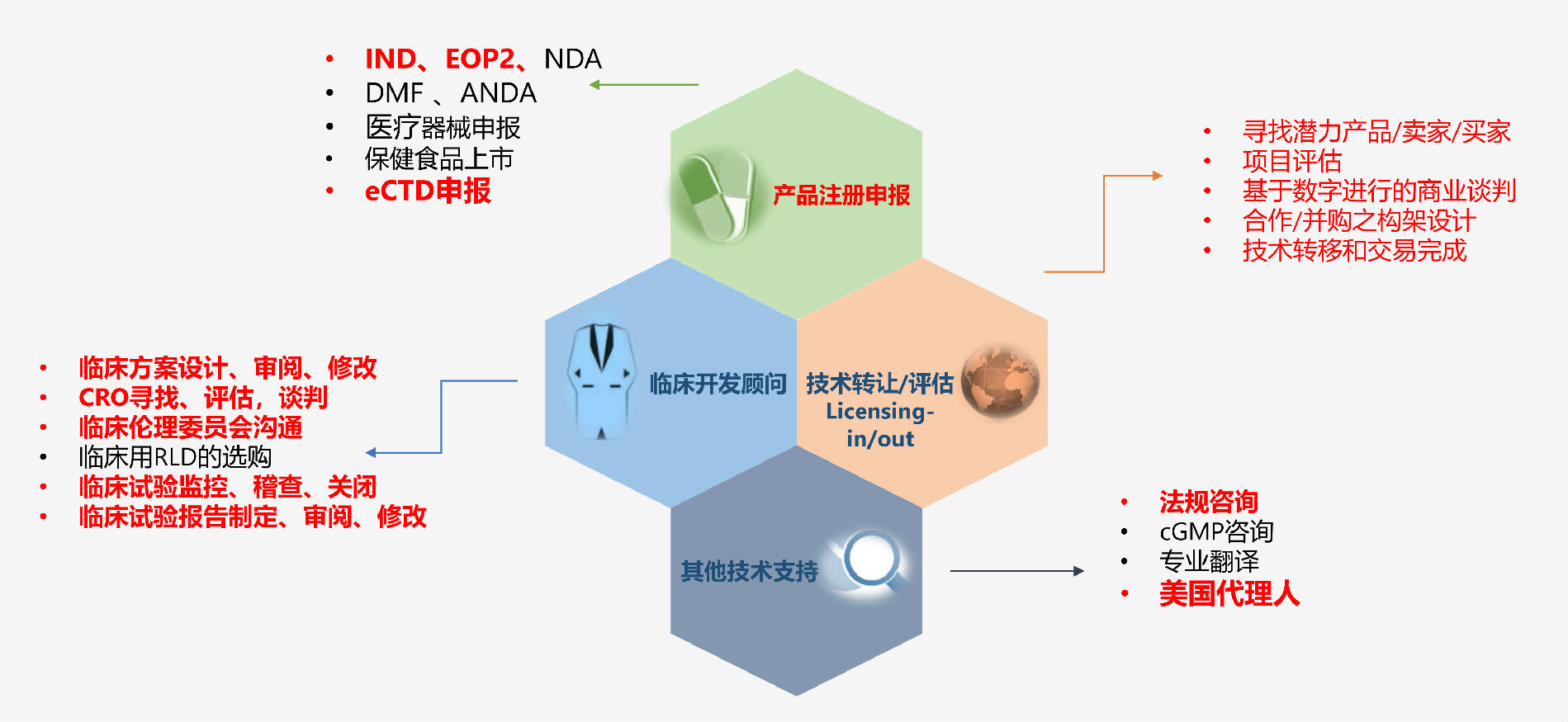
针对FDA所管辖的医药产品,从产品的研发、注册申报到市场开拓,可(kě)以提供一系列配套咨询服務(wù)。